Adenoma de Hipófisis - Información general
INTRODUCCIÓN
Los adenomas de hipófisis son tumores benignos de lento crecimiento que se originan en las células que forman a la glándula hipófisis.
La glándula hipófisis es considerada como la “glándula maestra” la cual regula la función de otras glándulas del cuerpo.
Los adenomas de hipófisis son relativamente comunes, ocurren aproximadamente en 1 de cada 1.000 adultos y son en su inmensa mayoría tumores benignos (no cancerosos) y de lento crecimiento.
Por el contrario, los carcinomas de hipófisis (tumores malignos) son extremadamente raros (menos del 0.2 % de los tumores de hipófisis).
Algunos adenomas de hipófisis, aunque siguen siendo benignos, pueden invadir las estructuras adyacentes (por ejemplo el seno cavernoso), sin que ello implique malignización.
Algunos datos epidemiológicos a tener en cuenta con respecto a los adenomas de hipófisis:
- Sexo: no existen grandes diferencias, afectando globalmente de igual manera a hombres y mujeres, aunque esto puede variar según el tipo de adenoma.
- Edad: existe una mayor incidencia entre la tercer y cuarta década de vida.
- Representan entre el 10-25% de los tumores intracraneales primarios en adultos y el 2% en población pediátrica.
- Incidencia:0.5 a 8.2 casos nuevos cada 100.000 habitantes por año.
- Prevalencia según reportes médicos: 1 caso cada 1064 habitantes.
CAUSAS DE LOS ADENOMAS DE HIPÓFISIS
Adenomas de Hipófisis Esporádicos
La mayoría de los adenomas hipofisarios se producen espontáneamente, es decir que no son hereditarios.
Si bien existen múltiples genes involucrados en el desarrollo y crecimiento de los adenomas de hipófisis, aún no se conoce una causa bien establecida. Muchos de estos genes y mecanismos moleculares son resorte de estudios permanentes en la actualidad (por ejemplo: metilaciones en los genes P16, DAPK, FGFR2, GADD45ɣ, MEG-3, etc.).
La alteración genética más comúnmente encontrada en tumores esporádicos es una mutación del gen gsp, un oncogén identificado en la mayoría de los adenomas secretores de GH. La mutación gsp se ha identificado en aproximadamente el 40% de los adenomas secretores de GH, pero es poco frecuente en otros subtipos de tumor hipofisario (ocurre en sólo el 10% de los adenomas hipofisarios no funcionantes y en el 5% de los adenomas corticotropos).
Lo que está demostrado es que los adenomas de hipófisis son de origen monoclonal. Es decir, que una única célula de la hipófisis se transforma, por causas aún no bien esclarecidas, en adenomatosa; se produce luego una serie de divisiones (mitosis) a punto de partida de esta célula y que llevan al crecimiento definitivo del adenoma.
Adenomas de Hipófisis Hereditarios
Los casos mucho más raros de adenomas de hipófisis con posibilidad de heredarse son en pacientes con algunos síndromes familiares complejos. En estos casos sí se han logrado identificar mutaciones genéticas bien claras que son las que producen el adenoma de hipófisis y el síndrome familiar. Alguno de los estos síndromes familiares son:
- Neoplasia Endocrina Múltiple Tipo 1 (gen MEN-1: 11q13).
- Neoplasia Endocrina Múltiple Tipo 4 (gen p27).
- Complejo Carney (gen PRKAR1A: 17q22-24).
- Síndrome de McCune-Albright (gen GNAS1: 20q13).
- FIPA (del inglés Familial Isolated Pituitary Adenoma, gen AIP: 11q13.3).
CLASIFICACIONES
Existen múltiples clasificaciones para los adenomas de hipófisis. Estas clasificaciones son de utilidad para los médicos especialistas endocrinólogos y neurocirujanos ya que les permite interpretar a cada uno de los pacientes de una manera simplificada. Se detallan a continuación las más frecuentes.
Clasificación según el Tamaño
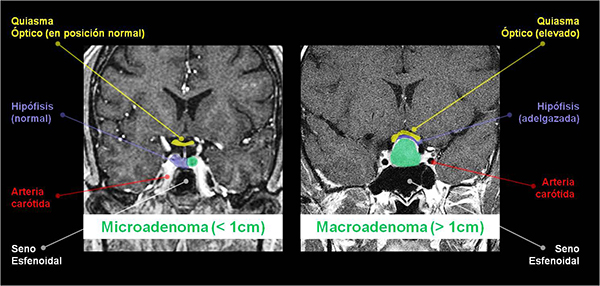
Según su dimensión los adenomas de hipófisis en la resonancia magnética se clasifican en:
- Microadenoma: menor a 10 milímetros de diámetro.
- Macroadenoma: mayor a 10 milímetros de diámetro.
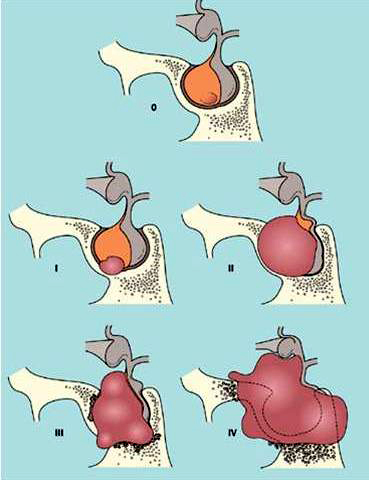
Clasificación de Hardy
Según el grado de invasividad local:
- Microadenomas
0: Apariencia hipofisaria normal
I: Microadenoma menor de 10 mm limitado a la silla turca
- Macroadenomas
II: Macroadenoma mayor de 10 mm limitado a la silla turca
III: Invasión localizada de la silla turca
IV: Invasión difusa de la silla turca
Clasificación de Hardy
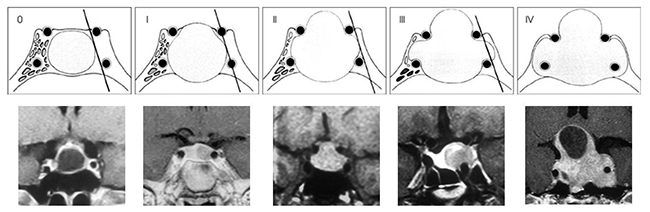
Clasificación de Knosp
Según el grado de invasión del adenoma en el seno cavernoso.
- Grado 0: el tumor no invade el seno cavernoso. Todas las estructuras anatómicas intracavernosas están preservadas. El tumor no sobrepasa la línea tangencial que une la pared medial de la arteria carótida interna supracavernosa con la carótida interna intracavernosa.
- Grado 1: el tumor sobrepasa la tangente medial (definida como la línea que une los dos bordes mediales de la carótida supra e intracavernosa) pero no sobrepasa la línea tangencial que une los dos centros de la carótida supra e intracavernosa.
- Grado 2: Se caracteriza porque el tumor se extiende sin sobrepasar la tangente que une los dos bordes laterales de la carótida supra e intracavernosa.
- Grado 3: el tumor se extiende lateralmente sobrepasando la línea tangencial lateral que une la porción carotidea supracavernosa con la intracavernosa.
- Grado 4: se caracteriza porque la carótida está totalmente englobada por el tumor.
Clasificación de Knosp
Clasificación Clínica-Hormonal
Existen dos grupos bien diferenciados de adenomas de hipófisis.
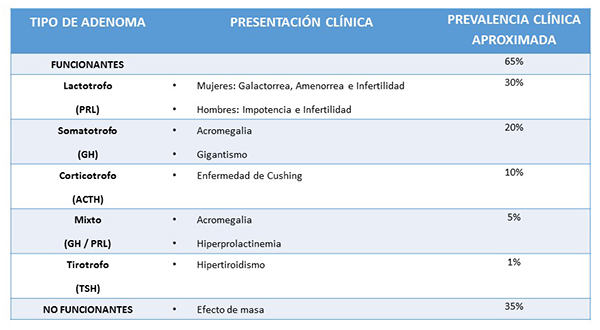
En el primer grupo (65%) encontramos a aquellos adenomas de hipófisis que por sus características producen la secreción excesiva de alguna hormona específica con determinada actividad y que producen una manifestación clínica característica. A este grupo se lo conoce como adenomas funcionantes.
En el segundo grupo (35%) encontramos a los adenomas de hipófisis que no producen una secreción excesiva de alguna hormona activa. A este grupo se lo conoce como adenomas no funcionantes.
Independientemente de si son adenomas funcionantes o no funcionantes, cuando el tamaño del tumor es importante se producen los síntomas asociados a compresión de estructuras adyacentes intracraneanas (efecto de masa).
Clasificación Anatomopatológica y por Inmunohistoquímica
Con las técnica clásica histológica (hematoxilina-eosina) se pueden apreciar distintos tipos de células (acidófilas, basófilas o cromófobas) dependiendo del tipo de adenoma que se esté analizando. Además, lo característico es una pérdida del patrón en cúmulos celulares, típico de la glándula hipófisis y también la desaparición de la red de reticulina.
Así, antiguamente se clasificaban a los adenomas en acidófilos, basófilos o cromófobos.
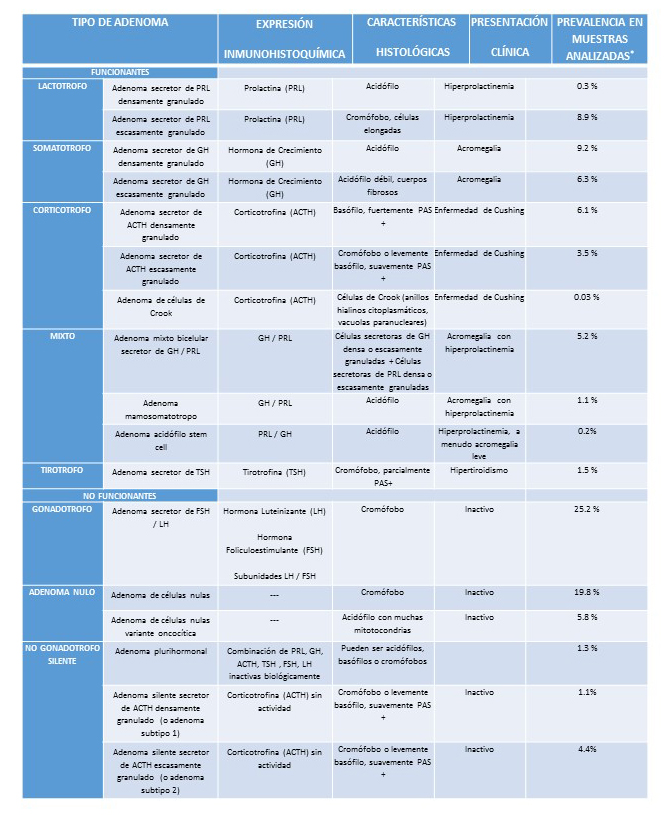
En la actualidad, solamente con la histología convencional no es suficiente, y el correcto diagnóstico final del tipo de adenoma debe establecerse por el análisis inmunohistoquímico.
Mediante la inmunohistoquímica es posible identificar el tipo de célula que le da origen al adenoma. Para ello, se utilizan anticuerpos que se unen específicamente a la hormona que se quiere investigar. Así, si un determinado adenoma sintetiza, por ejemplo GH; la inmunohistoquímica permitirá identificarlo con gran precisión y estaremos ante la presencia de un adenoma productor de hormona de crecimiento (acromegalia / gigantismo)
El análisis inmunohistoquímico es imprescindible luego de una cirugía de un tumor de hipófisis para poder definir qué tipo de adenoma de hipófisis fue el operado. Esto es fundamental para determinar el tratamiento en casoo de que no se logre la curación con la cirugía.
* Collection in the German Registry of Pituitary Adenomas of the years 1996–2005
Además, por inmunohistoquímica es posible identificar en los tumores de hipófisis algunos marcadores de actividad celular aumentada (índice Ki-67 y p53) que permiten determinar el pronóstico del adenoma.
- El antígeno Ki-67 es una proteína nuclear que se asocia la la proliferación celular y es un excelente marcador para determinar la fracción de crecimiento de una población celular dada. El porcentaje de células tumorales con Ki-67 positivos (índice Ki-67) a menudo se correlaciona con la evolución clínica de un tumor. En el caso de los adenomas de hipófisis el índice Ki-67 es de valor pronóstico para la recurrencia del tumor, y puede definir el tratamiento a seguir luego de una cirugía. En los informes de anatomía patológica se puede encontrar el índice MIB-1 que es el equivalente al índice Ki-67.
- La proteína p53 tiene una función antitumoral a través de mecanismos genéticos muy complejos. Normalmente está presente en células sanas a niveles muy bajos. En ciertos adenomas de hipófisis puede aumentar mucho su nivel y puede detectarse por inmunohistoquímica.
Es importante definir algunos términos en lo referente a los adenomas de hipófisis:
- Adenoma invasivo: se denomina así a aquellos adenomas que pueden invadir estructuras adyacentes a la silla turca (senos cavernosos, diafragma selar, piso de la silla turca, clivus). Que un adenoma sea invasivo no quiere decir que sea maligno. De hecho, alrededor del 50% de los adenomas presentan algún grado de invasión de las estructuras adyacentes.
- Adenoma agresivo: este término de perspectiva clínica, se reserva para aquellos adenomas invasivos que una vez tratados adecuadamente (fármacos, cirugías y/o radioterapia) persisten con un crecimiento tumoral y son de difícil tratamiento.
En el año 2004 la Organización Mundial de la Salud definió los siguientes tres tipos de adenomas de hipófisis en base a las características anatomopatológicas e inmunohistoquímicas:
- Adenoma de hipófisis típico (ICD 8272/0).
- Adenoma de hipófisis atípico (ICD 8272/1): es aquel que reúne todos los siguientes criterios: presenta invasividad, elevado índice mitótico, índice Ki-67 (MIB-1)>3% y, reactividad nuclear extensa para la proteína p53.
- Carcinoma de hipófisis (ICD 8272/3): es aquel adenoma de características similares al adenoma de hipófisis atípico pero sonde se demuestra la presencia de metástasis dentro o fuera del sistema nervioso central. Son muy raros (menos del 0.2 % de los tumores de hipófisis).
PRESENTACIÓN CLÍNICA: SÍNTOMAS Y SIGNOS
La presentación clínica de un adenoma de hipófisis dependerá de si el adenoma produce algún tipo secreción excesiva de hormona hacia la sangre (adenomas funcionantes) o bien no produce ni secreta hormona alguna (adenomas no funcionantes).
En el caso de los adenomas de hipófisis funcionantes, los pacientes generalmente experimentan síntomas relacionados con la acción de la hormona en exceso en el cuerpo. Así, existen diferentes tipos de adenomas funcionantes:
- Prolactinomas: secretan prolactina (PRL).
- Somatotrofos: secretan hormona de crecimiento (GH).
- Corticotrofos: secretan adrenocorticotrofina (ACTH).
- Tirotrofos: secretan Tirotrofina (TSH).
- Mixtos: habitualmente secretan GH y PRL.
Típicamente, los adenomas no funcionantes causan problemas relacionados con el tamaño del adenoma, el cual comprime a las estructuras circundantes. A esto se lo conoce como efecto de masa. Así, grandes adenomas pueden comprimir el quiasma óptico o los nervios ópticos, lo que lleva a la pérdida de la visión. También pueden comprimir a la glándula hipófisis normal y causar insuficiencia hipofisaria, es decir un déficit en la secreción normal de alguna de las hormonas de la glándula hipófisis (hipopituitarismo). Otra posibilidad, es lo que se denomina “efecto tallo”, que es una elevación leve a moderada de la hormona prolactina en respuesta a la compresión del tallo hipofisario por parte del adenoma. Por último, puede ser que el paciente refiera cefalea retrocular o bien holocraneana debido a la compresión de los receptores del dolor ubicados en la duramadre de la silla turca.
Cabe destacar también que los adenomas funcionantes pueden crecer y alcanzar algunas veces tamaños importantes, causando los mismos problemas de efecto de masa descritos anteriormente; además de los efectos relacionados con la propia hipersecreción hormonal.
Por lo antedicho, resulta muy importante un adecuado examen visual y la evaluación completa de la función hipofisaria cuando se diagnostica un adenoma de hipófisis.
Cefalea
Pérdida del campo visual.
DIAGNÓSTICO
Inicialmente, es imperiosa la elaboración de un adecuado examen clínico; con especial interés en los aspectos neurológicos, endocrinológicos y oftalmológicos. Por ello, es necesario el trabajo multidisciplinario entre neurocirujanos, endocrinólogos y oftalmólogos para poder arribar a un diagnóstico correcto.
Los exámenes complementarios incluyen:
- Resonancia Magnética de Cerebro con Foco en Hipófisis con Gadolinio
Es el método de elección para definir las características del adenoma, su tamaño y relación con las estructuras intracraneanas. Debe ser realizada bajo la administración de gadolinio, ya que de esta manera se mejora la sensibilidad del estudio. Según su tamaño, se clasifica a los adenomas hipofisarios en microadenomas (menores a 10 mm de diámetro) o macroadenomas (mayores a 10 mm de diámetro).
Los microadenomas suelen verse hipointensos en las secuencias T1 con gadolinio de la resonancia magnética, mientras que la adenohipófisis muestra una señal hiperintensa.
Los macroadenomas suelen ser hiperintensos en las secuencias T1 con gadolinio de la resonancia magnética, mientras que la hipófisis puede no distinguirse adecuadamente al estar adelgazada por el adenoma.
La neurohipófisis es de señal hiperintensa espontánea en secuencias T1 ya sean con o sin gadolinio.
En la actualidad existen equipos de resonancia magnética de una potencia de tres Teslas, los cuales brindan imágenes de altísima calidad y permiten detectar pequeños microadenomas de apenas algunos milímetros de diámetro.
Resonancia magnética que muestra un gran macroadenoma de hipófisis.
Laboratorio Hormonal Completo
Una evaluación endocrinológica determina los niveles de hormonas en sangre, orina o saliva para detectar niveles anormales causados por los adenomas de hipófisis. Pone de manifiesto el exceso de determinadas hormonas como así también si existe un déficit en alguna de ellas.
Las hormonas que habitualmente se dosan de manera rutinaria frente a un adenoma de hipófisis son las siguientes:
- Prolactina (PRL).
- Tirotrofina (TSH), Triiodotironina (T3), Tiroxina (T4): evalúan el eje de la glándula tiroides.
- Foliculoestimulante (FSH), Luteinizante (LH) , Testosterona, Estrógenos, Progesterona: evalúan el eje hipófiso-gonadal (ovarios o testículos).
- Adrenocorticotrofina (ACTH), Cortisol plasmático, Cortisol Libre Urinario (CLU), Cortisol salival: evalúan el eje hipófiso-adrenal (glándula suprarrenal).
- Hormona de crecimiento (GH), IGF-1.
Además, en ciertas circunstancias es necesario realizar dosajes hormonales mediante pruebas específicas. En estos casos es el médico endocrinólogo quien solicita el estudio. Un ejemplo de estudio dinámico puede ser el Test de Nugent para arribar al diagnóstico de la Enfermedad de Cushing.
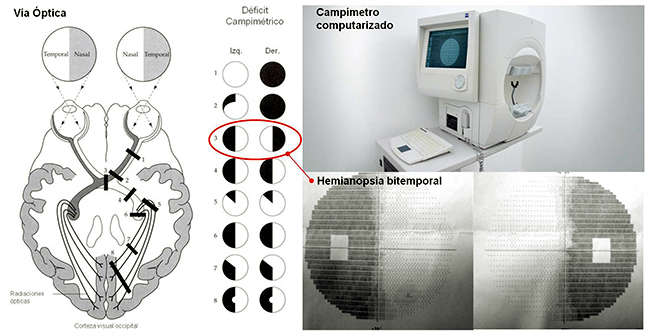
Campo Visual Computarizado
Permite determinar si existe algún compromiso en la vía óptica (nervios ópticos, quiasma óptico, cintilla óptica) por parte de un macroadenoma de hipófisis que la esté comprimiendo.
El cuadro clásico de pérdida del campo visual se conoce como hemianopsia bitemporal y se produce por una compresión del quiasma óptico por el macroadenoma. La hemianopsia bitemporal se caracteriza por una falta de la visión periférica mas lateral en ambos ojos y los pacientes solamente pueden ver lo que está justo enfrente de ellos. Muchos pacientes no se dan cuenta de su pérdida de visión hasta que es bastante avanzada.
También, pueden encontrarse otros déficits campimétricos que van desde cuadrantopsias superiores (imperceptibles por el paciente) hasta cuadros avanzados de amaurosis irreversibles.
Otros problemas visuales pueden incluir a la pérdida de la agudeza visual (visión borrosa o imposibilidad de enfocar correctamente) y la falta de la adecuada percepción de los colores. Por todo ello es necesaria una correcta evaluación neuroftalmológica en los macroadenomas.
TRATAMIENTO
El tratamiento óptimo de un adenoma pituitario depende de múltiples factores y una correcta interpretación de cada paciente de manera individual. Es necesario tener en cuenta:
- La producción excesiva de hormonas por el tumor (si existiere).
- El tamaño del tumor.
- Cuan invasivo es el tumor de las estructuras circundantes.
- La edad y la salud del paciente.
Los fármacos, la cirugía y la radioterapia solos o en combinación; son los pilares terapéuticos utilizados para tratar los adenomas de hipófisis y retornar los niveles hormonales a la normalidad.
Conducta Conservadora: Observación
Existen algunos adenomas de hipófisis que no producen síntomas ni alteraciones en los exámenes hormonales u oftalmológicos. Algunos se descubren incidentalmente al estudiarse el cerebro por otros motivos. Muchos de estos adenomas pueden permanecer estables durante largo tiempo y la simple observación mediante controles periódicos es la conducta a seguir.
Tratamiento Farmacológico
Los adenomas que producen hormonas hipofisarias deben ser tratados por un endocrinólogo especialista (neuroendocrinólogo).
Los prolactinomas suelen requerir sólo tratamiento farmacológico médico (no quirúrgico). Generalmente responden muy bien a determinados fármacos (cabergolina, bromocriptina), los cuales reducen el tamaño tumoral y normalizan los niveles de prolactina.
En el caso de la acromegalia y en la enfermedad de Cushing, si bien la cirugía es el tratamiento de elección inicial, la terapia farmacológica puede jugar un papel importante en el manejo hormonal pre y postoperatorio. Entre el arsenal farmacológico utilizado para la acromegalia se encuentran: Octreotide, Lanreotide, Cabergolina, Bromocriptina, Pegvisomant, Pasireotide. Estos medicamentos se utilizan asociados a la resección quirúrgica y también en los casos de tumores recurrentes o persistentes. En el caso de la enfermedad de Cushing, para el control de la producción de ACTH y/o cortisol antes o luego de la cirugía, el único fármaco aprobado es el Pasireotide; aunque en la práctica diaria se utilizan el Ketoconazol, la Cabergolina, el Mitotane y Aminoglutetimida, entre otros.Es igualmente importante abordar el hipopituitarismo,es decir la deficiencia que existe en la secreción normal de las hormonas hipofisarias, especialmente antes de la cirugía. En estos casos la terapia de reemplazo hormonal por parte del endocrinólogo es fundamental.
Cirugía
El tratamiento quirúrgico de los adenomas de hipófisis sigue siendo el más utilizado en la actualidad. La cirugía es, en líneas generales, la primera opción de tratamiento para los adenomas que producen enfermedad de Cushing, acromegalia o bien en los macroadenomas no funcionantes.
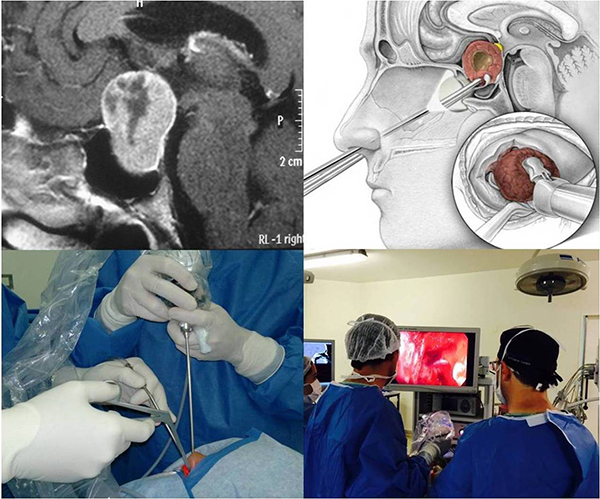
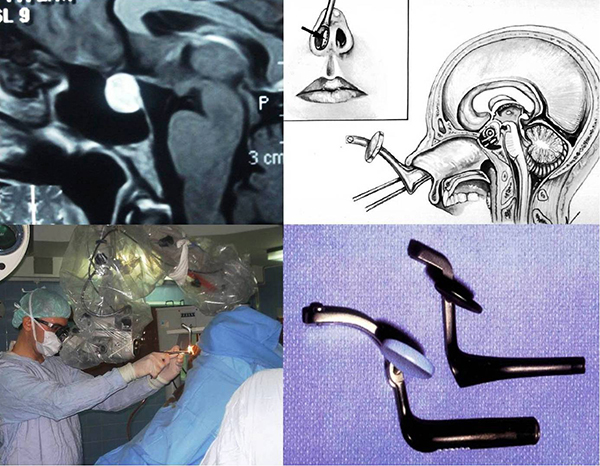
La técnica habitual se realiza, en la inmensa mayoría de los casos (96%), a través de la nariz en lo que se denomina cirugía transnasal transesfenoidal. La misma puede ser realizada con técnicas microquirúrgicaso por endoscopia, dependiendo de cada caso. La técnica endoscópica es la de mayor difusión en la actualidad.
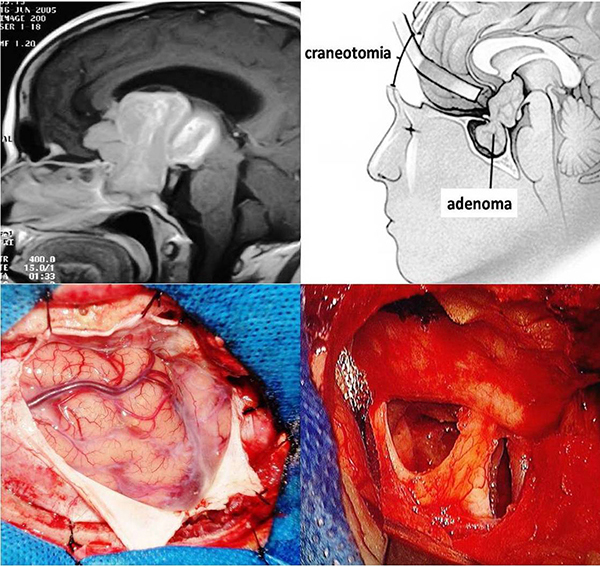
Menos de un 4% de los casos deben ser operados a través de una craneotomía mínimamente invasiva, es decir a través de una pequeña ventana ósea que se realiza en el cráneo. Este tipo de cirugía resulta de un grado mayor de complejidad que la cirugía transnasal transesfenoidal.
 |
 |
 |
Cirugía Transnasal Transesfenoidal.
|
Cirugía Transnasal Transesfenoidal.
|
Cirugía por Craneotomía. |
Radioterapia
La radiación funciona dañando el ADN dentro de las células haciéndolas incapaces de dividirse y reproducirse. Los beneficios de la radiación no son inmediatos, pero se producen con el tiempo. Poco a poco; el adenoma deja de crecer, disminuye su tamaño y función, y en algunos casos, desaparece por completo.
La utilización de la radioterapia queda reservada para aquellos casos de adenomas de hipófisis difíciles de tratar, en donde hay un fracaso de la cirugía y/o del tratamiento farmacológico. Es decir, como un complemento de alguna de dichas modalidades terapéuticas. Es por eso que la radioterapia hipofisaria no es la primera línea de tratamiento para los adenomas de hipófisis, y debe quedar criteriosamente indicada a través de un consenso entre el endocrinólogo y el neurocirujano.
Lo métodos actuales pueden ser:
- Radiocirugía estereotáctica: ofrece una alta dosis final de radiación distribuida en hasta cinco sesiones. Alguno de los equipos de dosificación de radiocirugía son el Gamma Knife, el LINAC, el Novalis, etc.
- Radioterapia estereotáctica fraccionada: libera una dosis baja de radiación durante varias sesiones diarias hasta recibir la dosis de radiación total en un plazo de 5 a 7 semanas.